хирургическое стадирование что это
Хирургическое стадирование что это
В настоящее время хирургическое стадирование выполняют не только как диагностическую процедуру, но и как стандартный метод лечения рака эндометрия (РЭ), за исключением тех случаев, когда сопутствующие заболевания служат противопоказанием. По данным последнего годового сообщения FIGO, среди 6260 больных раком эндометрия (РЭ) хирургическое стадирование выполнено в 94 % случаев.
Следует учесть, что учреждения, представившие данные для этого сообщения, были академическими; однако большинство пациенток с этой патологией, по крайней мере в США, оперируют не в академических лечебных учреждениях. Несмотря на твердо установленные принципы хирургического стадирования, некоторые специалисты полагают, что больным с низким риском метастазирования в лимфоузлы, т. е. с высокодифференцированными аденокарциномами (G1), лимфаденэктомия не показана.
Однако все больше данных свидетельствует о том, что при наличии высокодифференцированных опухолей по результатам гистологического исследования соскоба эндометрия у многих больных при исчерпывающем хирургическом определении стадии РЭ будут получены данные, которые существенным образом повлияют на дальнейшую тактику лечения.
Ben-Shacker и соавт. при обследовании 181 больной раком эндометрия (РЭ) с высокодифференцированными аденокарциномами обнаружили, что у 19 % имеются расхождения между степенью дифференцировки опухоли, определенной в соскобе эндометрия и установленной в результате гистологического исследования операционного материала; у 10,5% заболевание распространялось за пределы матки; у 3,9% выявлены метастазы в лимфоузлах и у 26% имелись факторы высокого риска, связанные с локализацией опухоли в матке.
Тщательное хирургическое стадирование показало, что 12% пациенток нуждались в адъювантной терапии и получили ее, а 17 % больных могли бы получить послеоперационное дополнительное лечение, которое им вовсе не показано. Geisler и соавт. сообщили, что из 349 больных с высокодифференцированными аденокарциномами у 15,9% обнаружены метастазы в лимфоузлах, причем у 2,6% — только в парааортальных. Из всех случаев метастазирования на долю высокодифференцированных (G1) опухолей приходится 31 %.
На основании этих и других исследований многие специалисты пришли к выводу о целесообразности проведения тщательного хирургического стадирования у всех больных раком эндометрия (РЭ). Последнее включает цитологическое исследование смывов из брюшной полости, двустороннюю тазовую и парааортальную лимфаденэктомию, а также абдоминальную гистерэктомию с двусторонней аднексэктомией. Безусловно, не следует забывать о необходимости тщательной ревизии органов брюшной полости с обязательной биопсией всех подозрительных участков.
Straughn и соавт. собрали данные о большом количестве больных, у которых стадии определены хирургическим методом. Стадия Ia (G1 и G2), характеризующаяся низким риском, диагностирована у 103 пациенток. Ни одна из них не получала послеоперационную терапию, и ни у одной не развился рецидив заболевания. К категории среднего риска авторы отнесли Ia (G3) и все случаи Ib и Iс стадий рака эндометрия (РЭ).
Из 440 пациенток у 93 % лечение ограничилось только операцией (1-я группа), у 5% возникли рецидивы. Послеоперационную ЛТ получило 28 пациенток (2-я группа), и только у 1 (4 %) возник рецидив. Среди больных 1-й группы впоследствии ЛТ провели только тем, у кого через разные промежутки времени после операции развились рецидивы; эффект был достигнут в 62 % случаев. По данным годового отчета (2003), 5-летняя выживаемость для Ia, Ib, Iс и IIа, IIb стадий после хирургического вмешательства составляла 93, 91, 73, 79 и 73 %, а после комбинированного лечения (операция + ЛТ) — 89, 91, 83, 83 и 75% соответственно.
Эти цифры показывают, что после комбинированной терапии выживаемость при Iс стадии рака эндометрия (РЭ) оказалась несколько лучше, чем после хирургического лечения. Какие факторы лежали в основе принятия решения о назначении ЛТ, неясно. В крупном многоцентровом исследовании рака эндометрия (РЭ) Iс стадии был установлен хирургическим методом у 220 больных. Пациенток с неблагоприятными гистологическими типами опухолей из протокола исключили. Адъювантную ЛТ провели у 99 (45%) больных, из них брахитерапию — у 56, ДЛТ на область таза — у 19, сочетанную ЛТ — у 24. Общая выживаемость больных раком эндометрия (РЭ) с патоморфологической Iс стадией после хирургического и комбинированного лечения была одинаковой (92 vs 90 %).
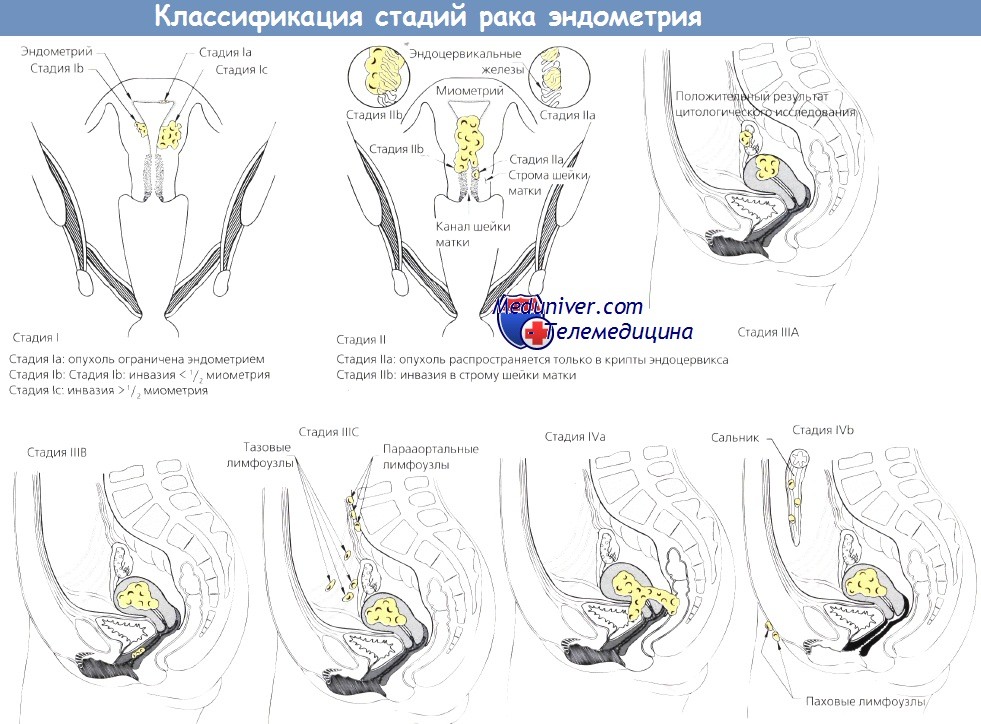
Классификация стадий рака эндометрия
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Стадирование рака
Правильное и эффективное лечение рака напрямую зависит не только от определения его типа, но и от сведений о размере опухоли и степени ее распространения.
Для систематизации такой информации во всем мире принято использовать международную классификацию стадий злокачественных новообразований TNM.
Классификация TNM основана на трех факторах: размер первичной опухоли (T — tumor), вовлеченность регионарных лимфатических узлов (N — nodes) и наличие отдаленных метастазов (M — metastasis). Для каждого вида рака существует своя градация, это определяет подход к лечению, а также прогноз.
Например, для рака молочной железы показатель T определяет диаметр первичной опухоли и ее взаимодействие с окружающими тканями. Опухоль с показателями Т1-Т3, ограниченная молочной железой, определяется размером, а T4, независимо от размера, предполагает распространение опухоли на кожу или грудную стенку. В то же время, для меланомы показатель Т определяется только глубиной прорастания опухоли (инвазия до 1 мм — Т1, а более 4 мм — Т4).
Показатель N для разных опухолей тоже разный, включая количество лимфатических узлов, их размеры, выход за предел капсулы лимфатического узла и т. д. N описывает только регионарные лимфатические узлы, которые отличны для каждой конкретной опухоли. Например, для рака печени лимфатические узлы вдоль ворот печени являются регионарными — ближайшими лимфатическими узлами, собирающими лимфу от области опухоли. Но, в то же время, расположенные рядом мезентериальные или забрюшинные лимфатические узлы, уже не являются регионарными для данной опухоли, а значит, определяются как отдаленные метастазы (М).
Ранее для каждого типа рака стадия определялась взаимоотношением этих трех параметров, но со временем, по мере изучения биологии рака и механизмов развития опухолей, параметров становилось все больше. Сейчас во всем мире используют классификации 8-го пересмотра, которые каждые 5-7 лет выпускают две организации: The Union for International Cancer Control (UICC) и The American Joint Committee on Cancer (AJCC).
Сегодня стадия может быть клинической (с), когда перед операцией мы определяем ее по данным диагностических исследований. Например, при раннем раке молочной железы стадия может выглядеть так — cT2N0M0. А после операции, когда весь материал был подвергнут полноценному гистологическому исследованию, выставляется патоморфологический диагноз (р), и этот же случай может быть рестадирован в pT2pN2а (5/12) M0. Это означает, что клинически неопределяемые метастазы в подмышечных лимфатических узлах были выявлены в 5 из 12 удаленных и исследованных лимфатических узлах.
Существуют и другие нюансы, возьмем, к примеру, стадирование после проведенной неоадьювантной (предоперационной) химиотерапии (префикс yp), когда у женщины с местнораспространенным раком молочной железы сT3N1M0 лечение начали с химиотерапии, а после провели операцию и увидели, что все опухолевые клетки погибли от химиотерапевтического лечения. Это означает, что у данной женщины полный лечебный патоморфоз, а стадироваться эта ситуация будет так — ypT0ypN0, CR.
Помимо TNM, используются также следующие символы:
Стадия может зависеть даже от того, определяется ли в опухолевой ткани вирус папилломы человека (p16), как это происходит в случае с раком ротоглотки.
Не все параметры используются для каждой опухоли, но процесс стадирования становится все сложнее. Этим мы обязаны прогрессу в лечении и большим данным, диктующим необходимость все более разных подходов для разных стадий.
Стадия также определяет прогноз, хотя и здесь подходы сегодня пересматриваются. Благодаря иммунотерапии, многие (ранее «безнадежные») пациенты с самыми последними стадиями онкологического заболевания получают возможность полностью избавиться от него на долгие годы. В то время, как пациенты с третьей стадией других болезней или даже того же вида рака, не отвечающего на иммунотерапию, неуклонно прогрессируют и умирают.
Пример: 2 пациента с идентичным распространением одного и того же вида рака толстой кишки, но у одного из них есть высокий уровень микросателлитной нестабильности — фактора ответа на иммунотерапию, а у другого нет.
Онкология, как и многие другие разделы медицины, сегодня обращена в сторону персонализации. И недалек тот день, когда стадирование будет осуществляться по иному принципу — не по степени анатомического распространения, а исходя из биологических особенностей конкретного заболевания.
Операции при раке яичников в Асаф ха-Рофэ
Отделение кардиологии и кардиохирургии
Отделение пластической хирургии
Лечение псориаза на Мертвом море
Лечение радиоактивным йодом
Отделение внутренних болезней
Передовые методы лечения

Хирургия предполагает применение лапаротомии, обширной абдоминальной операции.
Это основной диагностический инструмент, который также играет важную роль в лечении.
Кроме того, может использоваться лапароскопический подход.
Исследования показывают лучшие результаты у пациентов, особенно на поздних стадиях заболевания, которые получили медицинскую помощь в центрах, специализирующихся в лечении онкологии.
Очень важно, чтобы с женщиной работали высококвалифицированные онкологи.
Полное оперативное вмешательство включает:
Тип операции зависит в основном от размера опухоли и стадии болезни. Также влияет на выбор желание женщины иметь детей. Во время хирургии может быть выполнено несколько разных процедур наряду со стадированием. Развитие побочных эффектов будет зависеть от типа оперативного вмешательства.
Хирургическое стадирование при раке яичников в Асаф-ха-Рофэ
Стадия заболевания определяется во время операции. Хирургическое стадирование – важный этап, в процессе которого устанавливается тип и длительность лечения после операции. В некоторых случаях в ходе диагностики ранний этап болезни исправляется на более поздний.
Данная процедура включает проведение биопсии нижней части диафрагмы и сальника (жирового слоя, покрывающего органы брюшной полости), иногда лимфатических узлов вдоль брюшной аорты.
Если наблюдается аномальное накопление жидкости в полости брюшины, производится удаление асцита. Если данного побочного эффекта рака нет в настоящее время, выполняется абдоминальный смыв.
Он осуществляется путем введения солевого раствора в брюшную полость для облегчения обнаружения микроскопических злокачественных клеток, не видных невооруженным взглядом.
Затем хирург производит оценку таза и полости и удаляет раковые ткани, большую часть или весь сальник. Это касается и пораженного яичника, если врач полагает, что он содержит злокачественные клетки. Ткани отправляются в лабораторию для немедленной оценки.
Хирург исследует здоровый яичник:
Исследуется также кишечник и мочевой пузырь на предмет вторжения рака.
Органосохраняющие операции при раке яичников в Асаф-ха-Рофэ
После этого, как правило, рекомендуют проведение химиотерапии.
Исследования показывают, что при правильном и тщательном отборе пациенток, многим из них удается сохранить нормальную фертильность.
Однако большинство женщин с раком яичников не являются кандидатами для этой процедуры.
Цистэктомия – операция по удалению кисты, проводится на ранних стадиях заболевания, когда пациентка желает иметь детей в будущем.
Общая схема радикального хирургического вмешательства
Цель данной операции при раке яичников заключается в удалении максимального количества опухолевой ткани для улучшения симптомов и повышения эффективности химиотерапии. Хирургия выполняется следующим образом:
Операция циторедукция
Рак яичников распространяется путем посева злокачественных клеток по всей брюшной полости и зоне тазу. Уменьшение количества опухолевой ткани после операции улучшает прогноз заболевания.
Первичная циторедукция предполагает удаление максимально возможного объема опухоли. Основная цель – свести величину злокачественного образования до менее 1 см. Данная операция при раке яичников может включать:
Хирург также может поместить катетер в брюшную стенку для введения химиотерапевтических препаратов в полость.
Промежуточная (интервальная) циторедукция выполняется через 2-4 цикла химиотерапии, если лечение показало хорошие результаты. Ее рекомендуют пациенткам в случаях:
Паллиативные операции при раке яичников в Асаф-ха-Рофэ
Некоторые хирургические процедуры могут уменьшить симптомы и облегчить боль при метастазирующем раке яичников:
Лечение симптомов менопаузы

Они развиваются внезапно и могут быть более интенсивными, по сравнению с естественной менопаузой – раздражение, приливы, сухость влагалища, бессонница. Значительное количество женщин набирает вес.
Наиболее серьезные осложнения связаны с риском развития остеопороза и сердечно-сосудистых заболеваний.
В прошлом женщинам обычно назначали заместительную гормональную терапию после операции. Сейчас в связи с вероятностью возникновения рака груди и инсульта применение ЗГТ ограничили.
Решение об использовании экстрогензаместительной терапии отчасти зависит от возраста женщины и ряда других медицинских факторов. У молодых женщин (20-30-40 лет) преимущества ЗГТ для здоровья костей и сердца могут превосходить риски. У пациенток с возрастом ближе к менопаузе риски способны перевесить преимущества лечения. После овариэктомии женщине следует обсудить с врачом, подходит ли ей данный вид терапии.
Рак яичников-современный взгляд на проблему (по данным обзора литературы)
Среди множества патологических процессов наибольший интерес у теоретиков и клиницистов во все времена вызывали те из них, которые чаще всего приводили к гибели или инвалидизации больных. Без преувеличения можно сказать, что самым тяжелым и коварным заболеванием злокачественного генеза у женщин является рак яичников (РЯ). Проблема этой патологии была и остается одной из самых актуальных и трудных разделов онкологии, и поэтому широко обсуждается в различных областях медицины.
Рак яичников (РЯ) наряду со злокачественными опухолями шейки и тела матки является одним из наиболее распространенных заболеваний онкологической природы и в мировой статистике занимает третье место. По данным литературы, карцинома яичников составляет 6-8% из числа всех онкологических заболеваний и 20-25% среди злокачественных опухолей женских половых органов, причем рак яичников составляет около 80% всех опухолей придатков.
Анализ тенденций заболеваемости и смертности и их географических особенностей позволяет приблизиться к пониманию некоторых аспектов этиологии и патогенеза данного заболевания (Макаров О.В., 1996).
В настоящее время накоплено значительное количество экспериментальных, эпидемиологических и клинических фактов, позволяющих обозначить многие стороны этиопатогенеза РЯ, несмотря на это причины возникновения большинства опухолей яичников остаются неизвестными. Обзоры многочисленных исследований указывают на высокую частоту рака яичника в индустриальных странах, за исключением Японии. Возможно, это обусловлено диетическими факторами, а именно, высоким потреблением животных жиров, хотя последние исследования не подтверждают связи развития РЯ ни с высококалорийной пищей, ни с употреблением алкоголя, кофеина и никотина. Нет и убедительных доказательств возможного канцерогенного эффекта радиации, применяемой в диагностических и терапевтических целях, в развитии РЯ, хотя в эксперименте моделей опухоли яичника создавали путем облучения грызунов рентгеновскими лучами или при помощи пересадки ткани яичника в селезенку или другие органы портальной системы. В нескольких исследованиях развитие карцином яичников связывают с использованием талька в гигиенических целях.
Л.В. Акуленко с соавт. (1998) предложили критерии идентификации наслед-ственных форм РЯ. Таковыми являются:
Ранняя диагностика РЯ остается главной нерешенной проблемой в онкогинекологии. Клиническое ректо-вагинальное обследование малого таза нередко позволяет идентифицировать новообразование яичников. С 1970-х годов благодаря внедрению ультразвуковых технологий наступила новая эра в диагностике опухолей яичника. Ультразвуковое исследование малого таза стало рутинным методом в обследовании пациентки при подозрение на опухоль яичника. При небольших новообразованиях в малом тазу наибольшей информативностью обладает трансвлагалищная эхография, при образованиях более 6-7 см возрастает роль трансабдоминальной эхографии. Рак яичника на ранних стадиях эхографически представляет собой кистозное образование с единичными сосочковыми образованиями с нечеткими контурами, тогда как при 1С и ІІ стадиях уже визуадизируются обширные папиллярные разрастания с нарушением целостности капсулы кисты и в позадиматочном пространстве определяется небольшое количество жидкости. Для генерализованных стадий РЯ эхографически характерно наличие неправильной формы опухолевого конгломерата кистозно-солидного строения с размытыми границами разрастаниями по наружному контуру. Асцит выявляется в 70-80% набдюдений. При выявлении эхографических признаков злокачественности опухолевого процесса в яичниках и за их пределами необходимо дифференцировать первичность и вторичность поражения яичников.
Эхографические критерии дифференциальной диагностики первичного и метастатического рака яичников
Критерии: первичный рак, метастатический рак
Сторона поражения: чаще двустороннее всегда двустороннее
Структура кистозно-солидная: преимущественно кистозная Солидная,реже-с некрозом в центре
Размеры опухоли: свыше 10 см До 10 см
Контуры опухоли: нечеткие,неровные Четкие, бугристые
Связь с маткой: в конгломерате с маткой связь с маткой отсутствует
Современные стандарты лечения рака яичников были сформированы Интернацио¬нальной группой по изучению рака яичников на 7-ой международной конферен¬ции по онкогинекологии, проходившей в Риме в 1999.
При раке яичников различают пять типов хирургических вмешательств:
При ранних стадиях РЯ, к которым относят la, Ib и Па, в качестве хирургиче¬ского этапа лечения необходимо выполнять пангистерэкгомию с экстирпацией боль¬шого сальника на уровне поперечно-ободочной кишки. Для обоснования ранней ста¬дии, обязательно производится цитологическое исследование перитонеальной жидко¬сти, при её наличии, смывов с брюшины малого таза, боковых карманов брюшной полости, печени и диафрагмы. При низкодифференцированных опухолях необходима биопсия тазовых и парааортальных лимфоузлов. У молодых женщин с высокодиффе-ренцированным раком яичников или опухолями пограничной злокачественности, при желании пациентки сохранить детородную функцию, возможен органосохраняющий объем операции: односторонняя аднексэктомия с обязательной резекцией второго яичника, оментэктомией и цитологическим контролем. В подобных наблюдениях, которые чрезвычайно редки, после родов выполняют экстирпацию матки с оставшимися придатками. Следует помнить, что органосохраняющие операции при раке яичников — это исключение, а не правило.
Лапароскопия при подозрении на РЯ выполняется только в диагностиче-ских целях. Рядом авторов этот метод рекомендован для биопсии тазовых и парааортальных лимфатических узлов, как стандартный. Необходимо избегать неадек¬ватных лапароскопических вмешательств для хирургического лечения рака яич¬ников.
При подтверждении ранней стадии РЯ, адьювантная химиотерапия может не выполняться в случаях пограничной злокачественности и при высокодифференциро-ванном раке. В остальных случаях рекомендована комбинированная химиотерапия в количестве 4-6 циклов препаратами платины с алкилирующими агентами. Примене¬ние таксанов и антрациклинов при индукционной химиотерапии при ранних стадиях РЯ остается дискуссионным. Эффективность таких методов, как лучевая терапия и гормональное лечение при ранних стадиях РЯ не доказана.
При местно-распространенном и диссеминированном процессе, к которому ряд авторов причисляет и 1с стадию, в связи с наличием опухолевых клеток по брюшине, хирургическое вмешательство всегда должно быть этапом комплексно¬го лечения и носить циторедуктивный характер. Оптимальной циторедуктивной операцией считается субтотальная гистераднексэктомия или пангистерэктомия с экстирпацией большого сальника, с уменьшением остаточных опухолевых масс, по мнению разных авторов, от 0,5 до 2 см3. Только оптимальная циторедукция может быть основанием для постановки ШЬ стадии, при которой отдаленные ре¬зультаты заметно лучше, по сравнению с Шс стадией, в которой к сожалению, на¬ходится более половины больных, получивших комплексное лечение. В повседневной клинической практике встречают ситуации, когда полное удаление опухоли невозможно. Массивный канцероматоз, тотально замещенный опухолью “панцирный” большой сальник, прорастание опухоли в диафрагму, ворота печени и ее паренхиму, малый сальник, брыжейку тонкой кишки, забрюшинные пространства часто вынуждают хирурга минимизировать объем хирургического вмешательства. Вместе с тем, всегда следует стремиться к удалению первичной опухоли, большей части сальника и крупных опухолевых узлов на париетальной брюшине.
При Шс стадии объем вмешательства может быть уменьшен только из-за невозможности удаления масс опухоли без повреждения жизненноважных органов. Удаление лимфатических узлов забрюшинного пространства при РЯ, по мнению многих хирургов, носит диагностический характер. Дополнение операции аппендэктомией, спленэктомией, удалением пораженных отделов кишки, может проводиться только с целью достижения условной радикальности операции. Паллиативные вмешательства при нарастании кишечной непроходимости производятся с целью улучшения качества жизни больных. При массивных отдаленных метастазах в пе¬чень и легкие циторедуктивное вмешательство не показано. В свою очередь, около 10% больных раком яичников при первичном обращении оперировать не представляется возможным. Основными причинами подобных клинических ситуаций являются прорастание первичной опухоли в смежные органы и мягкие ткани малого таза, тотальный канцероматоз и множественные метастазы в органы брюшной полости, асцит, плевриты, отягощенное соматическое состояние, пожилой и старческий возраст, резко ослабленное состояние больных. Лечение этой категории больных начинается с системной полихимиотерапии. В результате короткого курса индукционной химиотерапии (2-4 цикла) примерно 30% больных представляется возможным выполнить промежуточную циторедуктивную операцию. Операция предпринимается с целью уменьшения массы первичной опухоли и ее метастазов и, таким образом, повысить эффективность последующей химиотерапии, а также улучшить качество жизни больных. Доказано, что промежуточная циторедуктивная операция повышает выживаемость больных раком яичников.
Прогноз больных раком яичников зависит, прежде всего, стадии заболевания (распространенности процесса), гистологического строения опухоли и плоидности опухолевых клеток. Далее следуют: степень дифференцировки клеток опухоли, экспрессия онкогена HER-2/neu, скорость размножения опухоли, размеры остаточной опухоли после хирургического вмешательства, выраженность асцита и возраст больной. Наиболее неблагоприятным прогнозом отмечаются больные с массивными диссеминированными формами злокачественных эпителиальных опухолей яичников. Полисерозиты и отдаленные метастазы у больных пожилого и старческого возраста, у которых верифицирован светлоклеточный или низкодифференцированный серозный рак с анэуплоидией клеток опухоли сводят шансы на излечение больной практически к нулю. В то время, как высокодифференцированные злокачественные опухоли яичников любого гистологического строения IА и IВ стадий излечиваются в 95-100% наблюдений. Приведенные факторы прогноза у больных запущенными формами рака яичников в связи с массивным распространением и большим суммарным объемом опухоли существенного прогностического значения не имеют, а любые методы лечения носят лишь паллиативный характер.
Статья добавлена 27 марта 2013 г.