Гранулематозное воспаление что это такое у женщин и как лечить
Хроническая гранулематозная болезнь
Хроническая гранулематозная болезнь — это редкая форма первичного иммунодефицита, при которой нарушается бактерицидная функция фагоцитов. Является наследственным заболеванием, в основном передается по Х-сцепленному рецессивному типу. Патология проявляется рецидивирующими инфекциями легких, ЖКТ, кожи и других органов. Для диагностики используется проточная цитометрия, генетическое тестирование, микробиологические исследования. Лечение включает антибиотикотерапию, противогрибковые препараты, иммуномодуляторы, в отдельных случаях рекомендована трансплантация костного мозга.
МКБ-10
Общие сведения
Заболевание известно с 1954 г. благодаря ученому C.A. Джейнвею и его коллегам, а генетические причины патологии начали изучаться только в 1980-х гг. Хроническая гранулематозная болезнь (ХГБ) встречается редко, в США ее регистрируют у 1 ребенка на 200-250 тысяч новорожденных. Данные по распространенности в России отсутствуют. Редкость проблемы, недостаточная осведомленность педиатров и терапевтов, сложности в подборе адекватной поддерживающей терапии — все это обуславливает большую актуальность этой хронической наследственной болезни в медицине.
Причины
Болезнь вызвана генетическими мутациями, которые передаются по наследству. Самым частым вариантом является Х-сцепленная мутация в гене gp91-фокс (60-70%). Болеют мужчины, а женщины являются носителями дефектного гена. Оставшиеся случаи приходятся на аутосомно-рецессивный тип наследования, связанный с генными мутациями p22-фокс, p47-фокс, p67-фокс. Этот подтипом заболевания могут страдать больные обоего пола.
Патогенез
В основе хронической гранулематозной болезни лежит дефицит НАДФН-оксидазного комплекса, который образуется при участии цитозольных и мембраносвязывающих белковых единиц. Вследствие мутации генов образование этих протеинов нарушается, в организме пациента не синтезируются ферменты, способные превращать молекулярный кислород в активные формы — супероксидный анион, перекись водорода, синглетный кислород.
Эти окислители в норме вырабатываются гранулоцитами (фагоцитами), составляют основу кислородозависимого этапа фагоцитоза. Он необходим для переваривания отдельных видов бактерий и грибков, продуцирующих фермент каталазу (например, Klebsiella sp, Candida albicans, Aspergillus niger). Остальные звенья клеточного иммунитета не нарушены, поэтому вирусные и паразитарные инфекции встречаются не чаще, чем в среднем в популяции.
Симптомы
Дети с ХГБ рождаются здоровыми, клинические признаки заболевания у них появляются в первые 2 года жизни. В атипичных случаях симптомы Х-сцепленного варианта хронической патологии манифестируют к 5 годам, а при аутосомно-рецессивном наследовании — к 9 годам. Основным признаком болезни являются инфекции, вызванные каталазоположительными Грам+ (Staphylococcus aureus) или Грам- бактериями (E. coli, Serratia liquefaciens, Klebsiella sp., P. aeruginosa, Proteus sp.).
Первичный иммунодефицит в 70-80% случаев манифестирует с рецидивирующих бактериальных инфекций дыхательных путей: тонзиллитов, бронхитов, пневмоний. Инфекционные заболевания отличаются тяжелым течением, умеренным ответом на стандартную антибиотикотерапию, частым переходом в нагноительные процессы. При этом образуются буллы, абсцессы, гангрена легкого.
В дальнейшем у 75-100% пациентов развиваются хронические гнойные лимфадениты, которые проявляются покраснением, припухлостью, болезненностью лимфоузлов. При поражении подмышечных или паховых узлов беспокоит резкая боль при движениях конечностями. В 24-41% случаев формируются гнойные воспаления печени, у 20-30% больных наблюдаются рецидивирующие желудочно-кишечные инфекции, бактериальные и грибковые поражения костей.
Характерным признаком гранулематозной болезни является генерализованный «бецежит», возникающий как осложнение после проведения первой прививки БЦЖ, проявляющийся спустя 1-2 месяца после иммунизации. Патология связана с недостаточностью клеточного иммунитета при введении ослабленных микобактерий Коха. Также после вакцинации есть вероятность начала остеита — формы костного туберкулеза.
Осложнения
Опасное последствие хронической гранулематозной болезни — аспергиллез легких, который провоцирует до 25% случаев смерти среди пациентов. Абсцессы печени чреваты развитием тяжелого гепатолиенального синдрома. Поражение костной ткани грибковым процессом, особенно в области позвоночника и ребер, сопряжено с массивной диссеминацией возбудителя, отличается крайне неблагоприятным прогнозом.
Типичным осложнением иммунодефицита у страдающих гранулематозной болезнью являются неконтролируемые микробные инфекции, которые распространяются по организму с возникновением сепсиса, септицемии, септического шока. При критическом снижении иммунитета, отсутствии своевременной помощи эти заболевания заканчиваются смертью больного. Также при гранулематозной болезни у детей отмечаются задержка роста, отставание в физическом развитии.
Диагностика
При первичной диагностике устанавливаются общие признаки иммунодефицита, выясняется семейный анамнез, степень риска генетической патологии. При физикальном осмотре патогномоничные проявления хронической гранулематозной болезни не определяются. Для постановки диагноза требуется комплексное лабораторно-инструментальное обследование:
Лечение хронической гранулематозной болезни
Консервативная терапия
При острых эпизодах микробных инфекций, возникших у пациентов с ХГБ, назначаются стандартные антибиотики из класса макролидов, цефалоспоринов, фторхинолонов. Для терапии грибкового поражения наиболее эффективен амфотерицин В, который принимается длительными курсами. Поддерживающее лечение, которые направлено на снижение риска инфекционных осложнений, включает следующие лекарства:
Экспериментальное лечение
Наиболее перспективным методом терапии больных хронической гранулематозной болезнью считается трансплантация гемопоэтических стволовых клеток, чтобы полностью восстановить нормальную иммунную защиту. Однако пересадка сопряжена с высоким риском осложнений, поэтому проводится ограничено в рамках исследовательских программ. На стадии разработки находятся различные методы генной терапии.
Прогноз и профилактика
Несмотря на применяемые методы лечения, нередко развиваются системные грибковые и бактериальные инфекции с летальным исходом. Прогноз относительно неблагоприятный, наблюдается ухудшение качества и снижение продолжительности жизни больных. Профилактика осложнений предполагает обеспечение постоянной поддерживающей терапии, проведение вакцинации в полном объеме (за исключением БЦЖ), максимальное ограждение пациента от инфекций.
Орофациальный гранулематоз
Орофациальный гранулематоз (ОФГ) характеризуется гранулематозным воспалением тканей лица и полости рта, при этом системное заболевание, вызывающее гранулемы, отсутствует.
Гранулематозное воспаление — это локальное воспаление, характеризующееся образованием гранулем (папул или узелков), вызванных несостоятельностью деятельности (трансформацией, пролиферацией) клеток, способных к фагоцитозу, играющих важную роль в иммунных реакциях и защите организма от инфекций.
Известны две клинические формы орофациального гранулематоза: гранулематозный хейлит Мишера (для него характерен стойкий или рецидивирующий отек нижней губы/губ) и синдром Мелькерссона — Розенталя (у него три клинических признака: рецидивирующий паралич лицевого нерва, складчатый или скротальный язык и стойкие отеки губ и периорбитальной области).
В некоторых случаях орофациальный гранулематоз может быть связан с такими заболеваниями, как саркоидоз, болезнь Крона и инфекционными заболеваниями (туберкулез).
ОФГ, возникающий сам по себе (не на фоне сопутствующих заболеваний) называют идиопатическим. До 40% пациентов с ОФГ имеют положительную реакцию при аллергопробах.
Распространенность орофациального гранулематоза неизвестна. По некоторым данным, она составляет всего 0,08% от общей популяции.
Причины
Причины возникновения орофациального гранулематоза точно неизвестны, однако предполагается, что заболевание связано с аномальным иммунным ответом у человека с предрасполагающими генетическими факторами. Считается также, что ОФГ может развиваться вследствие аллергических реакций — воздействия пищевых, контактных, лекарственных и других антигенов (бензоаты, ментол, глутамат натрия, коричный альдегид, додецилгаллат, золото, кобальт, ртуть).
Заболевание наблюдается и у мужчин, и у женщин, обычно развивается в молодом возрасте. Средний возраст манифестации ОФГ составляет 32 года, однако зарегистрированы случаи заболевания как возрасте 3 лет, так и в возрасте 78 лет.
Симптомы
Диагностика
Диагноз орофациальный гранулематоз устанавливается на основании физикального осмотра и симптомов (рецидивирующего отека ротовой полости или лица). И местные, и системные состояния, характеризующиеся гранулематозным воспалением, должны быть исключены соответствующими клиническими и лабораторными исследованиями. Подтверждает диагноз биопсия мягких тканей (губы или орофациальной области) с микроскопическим исследованием биоптата на неказеозные гранулемы.
Дифференциальный диагноз: приобретенный отек, связанный с дефицитом ингибитора C1-эстеразы, острые осложнения саркоидоза, болезнь Крона, абсцесс зуба, дерматологические проявления гранулематоза с полиангиитом или саркоидоза, гранулематоз с полиангиитом (гранулематоз Вегенера), гистоплазмоз, лепра, риноспоридиоз, эндокринная офтальмопатия, туберкулез.
Лабораторные исследования могут включать анализы на фолиевую кислоту, железо, витамин B12, ангиотензинпревращающий фермент, квантифероновый тест или кожную пробу на туберкулез. Для исключения саркоидоза врач может назначить анализ на определение антител к Saccharomyces IgA/IgG. Аллергопробы используются для исключения реакций на металлы, пищевые добавки и другие антигены.
Для исключения болезни Крона может быть назначена гастродуоденоскопия с прицельной биопсией и гистологическим исследованием, рентгенография/рентгеноскопия пищевода и желудка. Рентгенография органов грудной клетки или позитронно-эмиссионная томография могут назначаться, чтобы исключить саркоидоз и туберкулез.
Лечение орофациального гранулематоза
Орофациальный гранулематоз трудно поддается лечению. Оно сложное, растянуто во времени и направлено на устранение симптомов. Его эффективность окончательно не подтверждена. Лечение может включать глюкокортикоидную терапию (системную или введение препаратов непосредственно в очаг поражения) и нестероидные противовоспалительные препараты (для устранения отеков); антибиотики, иммуносупрессоры и хирургические методы (при стойких отеках, мешающих говорить и принимать пищу, а также для уменьшения давления на лицевой нерв). В случаях выявленной аллергии следует избегать контакта с антигеном. Соблюдение диеты (исключение корицы и бензоатов) может улучшить состояние пациента.
У пациентов с поражениями полости рта впоследствии может развиться болезнь Крона, поэтому необходима консультация гастроэнтеролога, иммунолога, диетолога. Чтобы исключить вероятное развитие болезни Крона и язвенного колита необходимо дальнейшее наблюдение.
Особенности и преимущества лечения орофациального гранулематоза в клинике Рассвет
Диагностика и лечение редких синдромов и болезней требует от врача глубоких и специфических знаний, помогающих правильно распознать орфанную патологию и назначить эффективное лечение.
Клиника Рассвет располагает современным и высокоточным оборудованием, позволяющим нашим врачам быстро и эффективно проводить диагностику и лечение любых состояний, в том числе таких редких заболеваний, как орофациальный гранулематоз. В нашей работе мы придерживаемся мультидисциплинарного подхода, поэтому при необходимости быстро подключаем к проблеме специалистов разных направлений: стоматологов, гастроэнтерологов, иммунологов, диетологов.
Рассвет — это доказательная медицина, лечение, основанное на международных протоколах, правильная коммуникация и поддержка пациентов.
Гранулема зуба
Гранулема зуба — это воспалительное образование на верхушке корня. Оно представляет собой разрастание грануляционной ткани. Гранулема формируется в результате действия защитных механизмов, при которых организм локализует очаг инфекции и стремится изолировать его от остальных тканей. По МКБ-10 болезни присвоен код К04.5.
Обычно гранулема образуется на фоне воспаления нервно-сосудистого пучка — пульпы. При отсутствии лечения пульпита воспаляется ее корневая часть, а инфекция выходит за пределы зуба, в околокорневые ткани. В результате формируется своего рода мешочек, заполненный продуктами распада погибших клеток.
Гранулемой считается образование размером до 0,5 см, но оно может расти, при этом по мере увеличения трансформируется в кистогранулему, размер которой достигает 1 см. При диаметре более 10 мм мы говорим о кисте корня зуба. В гранулеме нет полости, это участок тканей, окруженный капсулой. За счет последней гранулема прочно прикрепляется к верхушке корня зуба.
Причины развития патологии
Есть две причины развития гранулем на корне зуба.
1. Невылеченный пульпит. Развитие кариеса приводит к появлению глубокой полости в зубе. Патогенные микроорганизмы попадают в пульпу, она воспаляется, появляется сильная боль. Отсутствие врачебной помощи приводит к постепенному отмиранию пульпы. Бактерии проникают за пределы зуба через корневые каналы. У верхушки корня появляется очаг воспаления. Мы говорим о периодонтите.
Глубокая кариозная полость в этом случае наблюдается не всегда. Воспаление может развиваться внутри, при появлении вторичного кариеса под пломбой.
2. Некачественное эндодонтическое лечение. Гранулема может развиваться у корня зуба, в котором раньше проводилось пломбирование каналов корня. Обычно наблюдается недопломбирование: врач заполнил каналы материалом не до конца. В оставшихся пустотах развиваются болезнетворные бактерии, а окружающие корень ткани реагируют воспалением.
Эти причины вызывают большую часть случаев образования гранулемы. Но есть и другие, менее распространенные:
некачественное ортодонтическое лечение;
перенесенная травма зуба;
другие воспалительные заболевания — тонзиллит, абсцесс и др.
В последнем случае инфекция попадает в ткани с током крови или лимфы.
Симптомы гранулемы и осложнения
Симптомы гранулемы зуба неспецифичны. Часто пациент не подозревает о заболевании, поскольку признаки могут отсутствовать вовсе. Обычно зуб не беспокоит, но периодически возникает умеренная боль при надкусывании, употреблении горячих напитков или пищи. Такие симптомы свойственны всем формам периодонтита.
Стоит отметить, что время от времени заболевание может обостряться. Например, при переохлаждении, инфекционном заболевании, перенесенной операции — во всех случаях, когда снижаются защитные силы организма. При обострении появляются следующие симптомы:
острые боли, усиливающиеся при надкусывании, плотном смыкании челюстей;
отечность десны в проекции верхушки корня;
боль в десне при касании.
Обострение может проходить самостоятельно, а болезнь возвращается в хроническую форму. Но иногда воспаление развивается до появления гнойного содержимого в тканях — периостита или флюса.
Воспаление может стать причиной резорбции или рассасывания участка костной ткани челюсти. Появление гнойных осложнений опасно своими последствиями: от утраты зуба и поражения окружающих единиц до расплавления тканей и сепсиса. Поэтому важно получить своевременную помощь врача. Лечением гранулем зуба занимается стоматолог-терапевт, а если потребуется удаление, нужно обратиться к стоматологу-хирургу.
Особенности диагностики
Гранулематозное воспаление можно обнаружить только на рентгеновском снимке. Оно имеет вид затемнения у верхушки корня. Стоматолог проведет осмотр и ряд проб, после чего направит на прицельный снимок зуба. Снимок поможет не только поставить точный диагноз, но и увидеть размеры гранулемы, дифференцировать ее с другими формами периодонтита.
Консервативное лечение
При гранулемах чаще используется консервативное лечение. Оно состоит в механической обработке каналов корня. После этого они пломбируются временным лечебным материалом — пастами на основе гидроокиси кальция. Через 2−3 недели можно выполнить контрольный снимок, и если воспаление ликвидировано, каналы пломбируют постоянным материалом — гуттаперчей. На коронку зуба ставится новая постоянная пломба.
Есть две тактики лечения в зависимости от исходного состояния зуба.
1. Лечение гранулемы зуба, в котором не запломбированы каналы корня. В этом случае лечение предусматривает следующие этапы:
удаление кариозных тканей, старой пломбы на коронке, если она есть;
механическая обработка каналов — с помощью специальных инструментов они расширяются, сглаживаются стенки;
антисептическая обработка каналов.
Дальнейшие действия зависят от размеров гранулемы. Если она маленькая, до 3 мм, допускается одновременное пломбирование. Если образование больше 3 мм, то каналы корня пломбируются временной пастой. Она помогает гранулеме уменьшиться или исчезнуть полностью.
Ходить с временным материалом придется не больше 3 недель. По окончании срока врач направит на повторный рентгеновский снимок, и если увидит положительную динамику, пломбирует корневые каналы постоянным материалом. Также проводится восстановление коронки зуба.
2. Лечение зуба, в котором уже запломбированы корневые каналы. В этом случае врач сначала удалит старый материал. Если на зубе стоит коронка, она подлежит снятию. Каналы корня должны быть перепломбированы, а тактика лечения соответствует вышеописанной: иногда требуется установка временной лечебной пломбы.
Хирургическое лечение
Хирургическое лечение гранулемы зуба может потребоваться только в нескольких случаях:
непроходимость каналов корня — сложная, извилистая структура, слишком тонкие, узкие каналы;
невозможность распломбирования каналов;
наличие штифта в канале корня — попытки удаления могут стать причиной травмы;
нежелание пациента снимать коронку.
Многие пациенты предпочитают удаление гранулемы потому, что не хотят прибегать к долгому лечению и снимать хорошую коронку. В таком случае проводится операция резекции верхушки — часть корня удаляется вместе с гранулемой через небольшой разрез десны. Реже используется гемисекция — удаление одного корня многокорневого зуба вместе с частью коронки. В этом случае потребуется дальнейшее восстановление коронковой части зуба с помощью протеза.
В редких случаях зуб с гранулемой сохранять нецелесообразно. Например, если коронка сильно разрушена и ее нельзя восстановить. В этом случае врач, удаляя зуб, обязательно извлекает гранулему из лунки, чтобы не допустить развитие воспаления.
Если на фоне гранулемы развились гнойные осложнения, важно получить помощь врача незамедлительно. Специалист окажет первую помощь: снимет острую боль с помощью вскрытия зуба. Ранее запломбированные каналы вскрываются, через них впоследствии выводится гнойное содержимое. В этом случае облегчение наступает моментально.
Если появился сильный отек десны или щеки, это может быть связано с выходом воспалительного содержимого под надкостницу или слизистую оболочку полости рта. В этом случае выполняется небольшой разрез для выведения гноя. Дальнейшее лечение возможно только после купирования острых симптомов. Также потребуется медикаментозная терапия — врач назначит курс антибиотиков. Принимать их самостоятельно не стоит. Тем более бессмысленно лечиться только антибиотиками в надежде на то, что воспаление пройдет — они не способны устранить очаг заболевания и даже уменьшить его, важно принятие местных мер для ликвидации воспалительного процесса.
Особенности профилактики
Главным условием профилактики гранулем зуба является своевременная помощь стоматолога при появлении кариеса. Не стоит допускать сильного разрушения зуба, развития пульпита. Околокорневые ткани здоровы до тех пор, пока не воспаляется пульпа. Поэтому при появлении симптомов кариеса или пульпита важно срочно обратиться к врачу.
Эндодонтическое лечение также повышает вероятность развития периодонтита. Поэтому лучше ликвидировать кариес на ранних стадиях и не допускать необходимости пломбировки каналов корня. Если без этого не обойтись, важно внимательно выбирать стоматологическую клинику — профессионализм специалиста поможет исключить возможные ошибки и предупредить осложнения.
Современные представления о хронической гранулематозной болезни (ХГБ)
Хроническая гранулематозная болезнь (ХГБ) — достаточно неплохо изученное на сегодняшний день наследственное заболевание, связанное с недостаточностью фагоцитарной системы, следствием которой является иммунодефицит. Впервые ХГБ была описана в 1959 году у детей, для которых болезнь оказалась смертельной [1]. Болезнь не поддавалась лечению; на аутопсии выявляли генерализованное гранулематозное воспаление, отличающееся по своей специфике от известных на тот момент инфекционных и неинфекционных заболеваний.
Сегодня нам известно намного больше. Заболевание в большинстве случаев более не является смертельным, выявляется в основном у детей (врожденный иммунодефицит проявляется достаточно быстро), неплохо купируется. Однако до сих пор ХГБ относится к заболеваниям неизлечимым.
Этиология и патогенез
Сущность хронической гранулематозной болезни — в недостаточности фермента НАДФ-оксидазы, который представляет собой комплекс каталитических протеинов. Этот фермент, находясь в фагоцитирующих клетках, обеспечивает перенос электрона с НАДФ на молекулярный кислород: происходит т. н. «респираторный взрыв» (см. Рис. 1). Строго говоря, данный фермент есть не только у фагоцитов: единственным специфичным для них белком является трансмембранный gp91, остальные же компоненты встречаются в самых разных клетках [2].
Обратимся к рисунку 1. Белки gp91 и p22 объединяют в цитохром b558 — мембраносвязанную часть фермента НАДФ-оксидазы, остальные протеины называют цитозольными. При активации фагоцита различными медиаторами цитозольные p47 и p67 фосфорилируются и связываются вместе. Комплекс приобретает сродство к белкам p47 и rac2 — таким образом, присоединяясь к ним, данные протеины вызывают конформационные изменения в мембранном цитохроме b558, — и комплекс приобретает оксидазную активность [2, 5]. НАДФ-оксидаза переносит электрон от своего кофермента НАДФ на кислород с формированием активных форм кислорода (АФК) — O 2- и H2O2. Вот здесь и начинается самое интересное.
Классически считается, что фагоцит убивает микробы, образуя фаголизосому с бактерией или грибом, воздействуя на них большими дозами высокотоксичных АФК; однако в последнее время приобретает актуальность иная точка зрения. В 2002 году в Nature была опубликована статья, авторы которой пересмотрели всю парадигму деактивации поглощенных микробов.
Ученые обнаружили, что если в фагоцитах мышей определяется нормальный уровень активных форм кислорода, но имеется недостаточность лизосомальных ферментов — животные будут беззащитны против стафилококковых и кандидозных инфекций. То есть, несмотря на наличие нормального респираторного взрыва, иммунодефицит все равно присутствует. Стало быть, эффекторами в инактивации микроба являются не сами АФК [6].
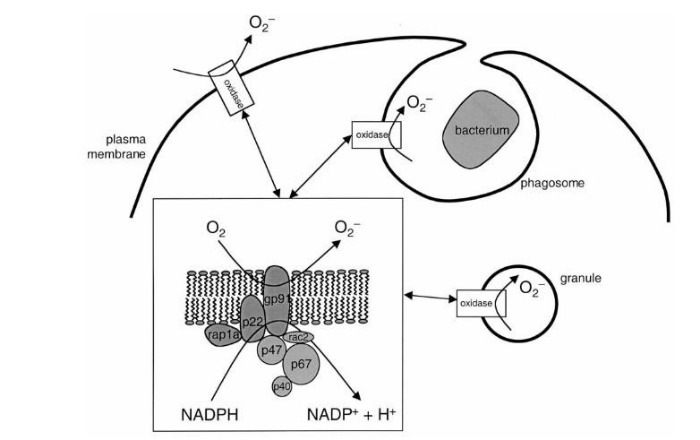
Согласно новой модели, АФК являются медиаторами в уничтожении микроба, а непосредственные «убийцы» — ферменты лизосом, обладающие протеолитической активностью. Как известно, при захвате фагоцитом микроба формируется вакуоль — (фагосома), с которой впоследствии сливается лизосома макрофага [7]. На мембране этой вакуоли и функционирует НАДФ-оксидаза, постоянно увеличивая концентрацию АФК. Однако как уже было сказано, данный процесс — не конечный эффекторный механизм.
Наследование и генетика
Хроническая гранулематозная болезнь имеет наследственную природу. Приблизительно данной патологией страдает 1 на 250 000 [9], что делает заболевание достаточно редким и потому трудным в диагностическом отношении. Заболевание вызывает мутация любого из четырех генов, кодирующих субъединицы ключевого фермента фагоцитоза НАДФ-оксидазы. Более двух третей случаев связаны с X-сцепленным наследованием (дефект гена CYBB, кодирующего белок p-91); остальные случаи связаны с аутосомно-рецессивным наследованием генов CYBA, NCF-1 и NCF-2, кодирующих белки p22, p47 и p67 соответственно. Исходя из этого болезнь обозначают как ХГБ X91, A22, A47 и A67 (в зависимости от типа наследования и локуса гена) [10].
Примечательно, что в литературе нет (или крайне мало) доказанных случаев наследственного дефекта других субъединиц. Однако в последнее время обнаруживаются все новые мутации генов, следствием которых становится ХГБ: например, в 2009 году выделили еще один подвид ХГБ, связанный с аутосомно-рецессивной мутацией гена p-40 [11], имеются также сведения о единственном пациенте с недостаточностью белка Rac2 — [10]. Вполне вероятно, что могут существовать и другие генетические патологии, вызывающие данное заболевание.
Диагностика
Диагностика ХГБ основана на выявлении клинических признаков, кроме того, важно выявить наличие или отсутствие респираторного взрыва. Последнее можно осуществить несколькими гистологическими и иммунологическими методами, например, окрашивание нитросиним тетразолием (НТЗ) позволяет определить, вырабатывают ли клетки АФК — НТЗ будет утилизироваться активными формами кислорода, в результате чего из бледно-желтого тетразолия образуется голубой формазан [12].
Среди наиболее ярких клинических симптомов можно выделить: пиодермию, пневмонию, воспалительные процессы желудочно-кишечного тракта, лимфаденит, абсцесс печени и остеомиелит [13] на фоне рецидивирующих бактериальных и грибных инфекций.
В крови выявляется гипергаммаглобулинемия и анемия. В местах дренажей — хроническое воспаление с образованием гранулем. Также гранулемы могут формироваться в различных тканях и органах: например, в желудке гранулематозное воспаление способно привести к обструкции желудочного канала, в урогенитальном тракте — к циститу. Также следует упомянуть, что почти 20 % больных ХГБ страдает от гранулематозного колита, который легко перепутать с болезнью Крона [14].
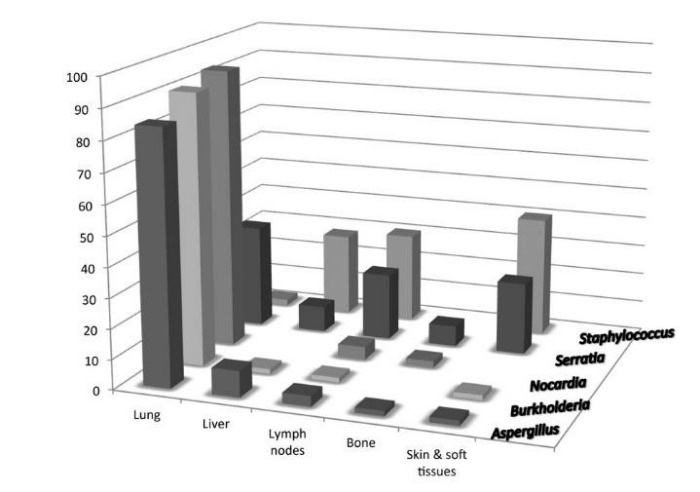
Также следует упомянуть о недавно открытой бактерии, выявленной у пациентов с ХГБ, которую исследователи предложили назвать Granulobacter bethesdensis. Это грамотрицательная палочка, которая на данный момент не может быть отнесена ни к одной из существующих таксономических групп; бактерия поражает лимфоузлы, кроме того, резистентна к антибиотикам in vitro и, скорее всего, — in vivo [18, 19]. Предполагается, что это — лишь первая из подобных бактерий, возникшая в эру антибиотиков. На данный момент Granulobacter bethesdensis не слишком распространена, однако имеет к этому весьма опасную тенденцию.
Лечение
В настоящее время активно разрабатываются методики, которые смогут не просто позволить больным с ХГБ жить полноценно, но и в перспективе совершенно избавить их от бремени заболевания. Поскольку болезнь наследственная, крайне трудно придумать что-то существенное, однако такие попытки предпринимаются, и некоторые из них обнадеживают.
Одна из них — лечение хронической гранулематозной болезни с помощью генной инженерии [20]. В 2006 году в Nature Medicine была опубликована статья, авторы которой сообщили об успешной коррекции генома двух пациентов с X-сцепленной формой ХГБ. После лечения у пациентов определяли активность нейтрофилов с помощью позитронно-эмиссионной томографии, а также других инструментальных методов. Исследование показало, что в обоих случаях фагоциты после проведенного лечения смогли оказать сопротивление инфекции. На данный момент это — одна из самых многообещающих методик.
Еще одним способом терапии является пересадка гемопоэтических клеток [21]. Двадцати семи пациентам после миелоаблативного режима кондиционирования (подготовка пациента к трансплантации с помощью лучевой или цитостатической терапии — прим. автора) пересадили гемопоэтические стволовые клетки от наиболее подходящих доноров (по белкам HLA — главного комплекса гистосовместимости). Двадцать три пациента вполне успешно перенесли операцию, а дальнейшее наблюдение позволило говорить об излечении этих пациентов от хронической гранулематозной болезни. Однако еще 4 пациента умерли от последующих инфекций (15 %).
В остальном же современная медицина может предложить крайне немного. Это — патогенетическая и симптоматическая терапия с использованием антибиотиков, дренажей и прочего. Излишне говорить, что подобное лечение не способно избавлять пациентов от ХГБ.
Профилактика инфекций.
Крайне важно предотвращение развития инфекционного процесса. Пациенты с ХГБ испытывают невероятные трудности в повседневной жизни, например, некачественная чистка зубов спокойно может окончиться гингивитом, а царапина — тяжелой бактериемией. Потому больным необходимо тщательным образом следить за гигиеной, выполнять профессиональную чистку зубов, обрабатывать все царапины антисептиком. И, разумеется, такие пациенты должны быть привиты по всем правилам [14]. В противном же случае даже достаточно простая инфекция может окончиться летально.
Источники: